
Unifesp - 2ª fase - Específicas
Obter energia é vital para todos os seres vivos, tais como as bactérias, os protozoários, as algas, os fungos, as plantas e os animais. Nesse processo, a energia é armazenada na forma de ATP, a partir de doadores e de aceptores de elétrons. Em certos casos, organelas como as mitocôndrias são fundamentais para o processo.
a) Dos organismos citados, quais são os que possuem mitocôndrias?
b) É correto afirmar que, tanto na fermentação quanto na respiração aeróbica, o doador inicial e o aceptor final de elétrons são moléculas orgânicas? Justifique.
a) Mitocôndrias são organelas que, segundo a Teoria da Endossimbiose ou Teoria endossimbiótica, apresentam ancestralidade comum com algumas bactérias. Isto quer dizer que as mitocôndrias possuem estruturas e características genéticas semelhantes a alguns seres do Reino Monera. Pode-se concluir, portanto, que estas organelas são aproximadamente do mesmo tamanho de uma bactéria e, apresentam funções bastante semelhantes. Sendo assim, conclui-se que é física e fisiologicamente impossível existir uma mitocôndria dentro de uma bactéria.
Entendemos, então, que segundo a mesma teoria supracitada, apenas os seres conhecidos como eucariontes teriam essa organela. Isto porque estes seres apresentam ancestralidade comum com células maiores, nucleadas, que provavelmente englobaram as antigas bactérias (ancestrais das mitocôndrias) com as quais passaram a viver em simbiose, dando assim origem às famosas mitocôndrias. Os seres vivos citados no texto, exceto as bactérias, são eucariontes e, portanto, todos apresentam mitocôndrias. São eles os protozoários, as algas, os fungos, as plantas e os animais.
b) Conhecendo-se os processos de fermentação e respiração aeróbica, não está correto afirmar que o doador inicial e o aceptor final de elétrons são, todos, moléculas orgânicas. Em se tratando apenas do doador inicial de elétrons, a afirmativa seria verdadeira, pois estaria tratando do reagente imprescindível para a ocorrência dos dois fenômenos, a glicose, que é uma molécula orgânica. Lembramos aqui que a glicose é um carboidrato (monossacarídeo) formado pelo encadeamento de seis carbonos (hexose) e, como todos os carboidratos ou glicídios, é classificada como uma molécula orgânica.
É ela que, no início da fermentação ou da respiração aeróbica (etapa conhecida por glicólise), é quebrada enzimaticamente em duas moléculas de três carbonos, chamadas piruvato. É importante ressaltar que esta quebra sofrida pela glicose até o piruvato é um processo longo que envolve fenômenos de fosforilação e oxidação do carboidrato.
Nota: Na realidade, durante a glicólise, a molécula de glicose é quebrada em duas moléculas de gliceraldeído-3-fosfato (G3P), sem perda de elétrons, antes de formar as duas moléculas de piruvato. Em seguida, o G3P é oxidado liberando elétrons. Esta é a primeira perda verdadeira de elétrons que ocorre nos fenômenos respiratórios e, portanto, conclui-se que o G3P é o real doador inicial de elétrons. Como a formação e transformação do G3P é uma etapa muito específica e pouco citada na literatura do Ensino Médio, imagina-se que a banca da Unifesp faz referência glicose como o doador inicial de elétrons, como explicado antes desta nota.
Ao ser oxidada, a glicose perde elétrons que são assimilados pelo carregador NAD+, uma coenzima que pode ser reduzida com dois elétrons e, aceitando um próton (H+), transforma-se no NADH. Esse irá transferir os elétrons a outras moléculas orgânicas, reduzindo-as e regenerando, assim, o NAD+, que pode ser reutilizado. É a partir deste ponto que a fermentação diferencia-se da respiração aeróbica.
Na fermentação láctica, a molécula que recebe os elétrons do NADH é o próprio piruvato, formado ao final da glicólise, enquanto na fermentação alcoólica a molécula que recebe os elétrons do NADH é uma molécula de dois carbonos oriundo da descarboxilação do piruvato, o acetaldeído. Nestes casos em que o piruvato, além de sofrer redução, também sofre descarboxilação, ocorre geração de CO2 e de outro produto, como o acetaldeído.
Ao serem reduzidos, o piruvato e o acetaldeído são transformados em algumas outras substâncias, dependendo do organismo que está realizando o processo. Na fermentação alcoólica, por exemplo, o acetaldeído é reduzido a etanol. Já na fermentação láctica, o piruvato é reduzido gerando lactato, sem produção de CO2.
Desse modo, como as substâncias derivadas da redução do piruvato ou do acetaldeído, feita pelo NADH (às vezes junto à descarboxilação), são produtos finais das suas respectivas fermentações, podemos concluir que o piruvato e o acetaldeído são os últimos aceptores de elétrons nos processos de fermentação citados. Sabendo que o piruvato e o acetaldeído são moléculas orgânicas, a afirmativa da questão estaria certa, se não fosse pelo que ocorre na respiração aeróbica.
Na respiração aeróbica o NADH, formado ao final da glicólise, não doa seus elétrons para um aceptor final, mas sim para uma proteína presente nas cristas mitocondriais (NADH-desidrogenase), componente da cadeia transportadora de elétrons (nome dado à última etapa da respiração aeróbica).
Nesta cadeia enzimática, elétrons são transferidos a moléculas proteicas que são sempre mais eletronegativas que sua “vizinha” anterior.
Assim, prótons de hidrogênio são lançados para a região intermembranas da mitocôndria gerando uma diferença de potencial desta região com a matriz mitocondrial.
Desse modo, os hidrogênios começam a ser captados de volta para a matriz, por uma enzima que realiza esta difusão, chamada ATP-sintase. Esta é a enzima que gera ATP à medida que vai recaptando os prótons de hidrogênio (Teoria quimiosmótica).
Ao final de todo o processo, os elétrons que chegam ao final da cadeia, descarregados energeticamente, são assimilados pela molécula do gás oxigênio (O2). Este é, portanto, o aceptor final de elétrons e, esta molécula, não é orgânica.
Enfim, após receber quatro elétrons o gás oxigênio aceita, também, quatro prótons de hidrogênio, gerando duas moléculas de água residuais, segundo a equação:
O2 + 4e- + 4H+ --> 2 H2O
Aparecera como um bicho, entocara-se como um bicho, mas criara raízes, estava plantado. Olhou as quipás, os mandacarus e os xiquexiques. Era mais forte que tudo isso, era como as catingueiras e as baraúnas. Ele, sinhá Vitória, os dois filhos e a cachorra Baleia estavam agarrados à terra.
(Graciliano Ramos. Vidas Secas, 1996.)
O trecho menciona algumas árvores da Caatinga (catingueiras e baraúnas), local em que muitas plantas, durante longos períodos de seca, permanecem sem as folhas, que são os principais órgãos fotossintetizantes dos vegetais. No entanto, imediatamente após a primeira chuva, essas árvores rapidamente se cobrem de ramos e folhas verdes.
a) Considerando que tais plantas permaneceram longos períodos sem folhas, de onde provém a energia necessária para a produção rápida de biomassa das folhas novas?
b) É válida a afirmação de que, com relação à pluviosidade, a Caatinga e o Cerrado apresentam os mesmos regimes de seca e de chuva ao longo do ano? Justifique.
a) A vegetação de Caatinga é composta por muitas espécies decíduas, ou seja, que perdem folhas durante a estação seca. Para a rebrota destes vegetais é necessária a utilização de carboidratos, especialmente o amido, armazenados em parênquimas amilíferos, mais frequentemente encontrados nas raízes desses vegetais, mas que podem ser encontrados também nos caules.
b) A afirmação não é válida, pois os regimes de chuva e de estiagem na Caatinga e no Cerrado são bem diferentes. A caatinga, caracterizada pelo clima semi-árido, apresenta precipitação anual inferior a 1000 mm. Chove de 2 a 4 meses, restando 8 a 10 meses de seca. No cerrado, a precipitação média anual fica entre 1200 e 1800mm, sendo os meses de março e outubro os mais chuvosos. Durante a primavera e o verão, curtos períodos de seca, chamados veranicos, podem ser observados. Entre maio e setembro, as taxas de chuva reduzem bastante.
Cantiga para adormecer Lulu
Lulu, lulu, lulu, lulu,
vou fazer uma cantiga
para o anjinho de São Paulo
que criava uma lombriga.
[…]
A lombriga devorava
seu pão,
a banana, o doce, o queijo,
o pirão.
[…]
Lulu, lulu, lulu, lulu,
pois eu faço esta cantiga
para o anjinho de São Paulo
que alimentava a lombriga.
(Cecília Meireles. Ou isto ou aquilo.)
No poema, a autora descreve a lombriga (Ascaris lumbricoides) no singular, como se fosse um único indivíduo, como ocorrem com as solitárias (Taenia solium). Diz, também, que a lombriga devorava todo alimento ingerido por Lulu.
a) Lombrigas e solitárias (tênias) não pertencem ao mesmo filo animal. Ao comparar o processo digestivo das lombrigas e da solitária, constata-se que o mais parecido com o dos seres humanos é o das lombrigas. Que características do filo das lombrigas e do filo da solitária permitem tal constatação?
b) Em geral, o alimento do hospedeiro já chega digerido até a lombriga e a solitária. Uma vez ingeridos, de que maneira os nutrientes são distribuídos a todas as partes do corpo desses animais?
a) Solitária é o nome popular dos animais pertencentes ao gênero Taenia, parasitas do trato gastrointestinal de vertebrados. Este gênero pertence ao filo Platyhelmintes. Lombriga é o nome popular pelo qual são chamados os parasitas humanos do gênero Ascaris, alocados no filo Nematoda. A estrutura do trato digestório nestes animais é bastante diferente e sua comparação é a chave para que o candidato chegue à constatação sugerida pelo enunciado.
Os Platyhelmintes são animais que tipicamente possuem um sistema digestório incompleto. Este tipo de organização do sistema digestório consiste em uma cavidade digestiva (frequentemente chamada de cavidade gastrovascular), associada a uma única abertura, por meio da qual o alimento entra e os restos de alimento não digeridos saem do aparelho digestório.
Já os Nematoda apresentam o que se chama de sistema digestório completo. Essa arquitetura de sistema digestório compreende uma organização em tubo, com duas aberturas: uma anterior (por onde é ingerido o alimento) e outra posterior (através da qual saem os restos da digestão).
Humanos são Cordados, que, assim como os Nematódeos, apresentam sistema digestório completo. Dessa forma, podemos constatar a maior similaridade entre o sistema digestório de humanos e lombrigas.
Nota: O enunciado faz referência às solitárias, mas pede comparações entre os sistemas digestórios do filo a que pertence este animal e do filo a que pertencem as lombrigas. Dessa forma, é necessário lembrar que o candidato deveria apontar as diferenças relacionadas ao sistema digestório incompleto, característica do filo Plathyelmintes, embora as Tênias, em particular, devido ao modo de vida parasita, não tenham sistema digestório.
b) A questão pede que o candidato compare a circulação de substâncias em Plathyelmintes e Nematoda. Nos Plathyelmintes não há sistema circulatório. Dessa forma, a absorção dos nutrientes já digeridos pelo hospedeiro se dá por toda a superfície do corpo do animal e a distribuição de nutrientes se dá por transporte passivo, célula a célula.
Já nos Nematoda, a absorção se dá por meio do epitélio de revestimento do tubo digestório. A partir deste epitélio, os nutrientes chegam ao pseudoceloma, uma cavidade corporal preenchida por fluido, o líquido pseudocelomático. Além de funcionar como esqueleto hidrostático, fornecendo sustentação à musculatura e proporcionando movimento, o líquido pseudocelomático é o responsável pela distribuição, ao longo do corpo do animal, dos nutrientes provenientes do alimento.
A figura representa os sistemas digestivos de dois mamíferos, um herbívoro não ruminante e um carnívoro estrito.
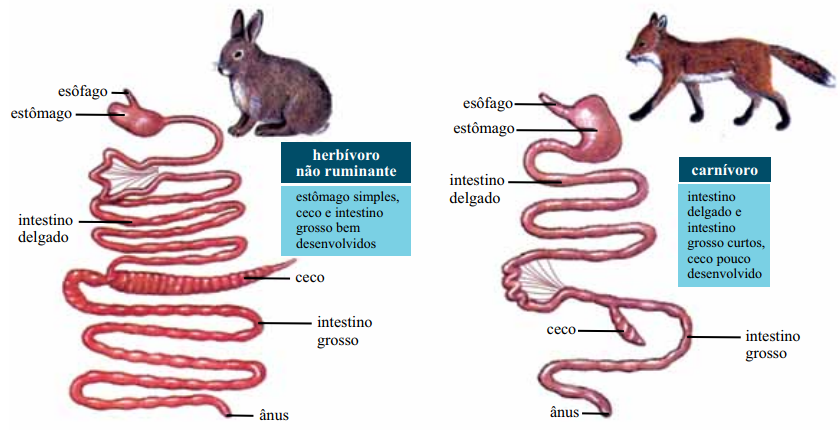
(Cleveland P. Hickman et al. Princípios Integrados de Zoologia, 2013. Adaptado.)
a) Considerando a dieta de cada um dos animais, explique por que os intestinos do herbívoro são consideravelmente mais longos do que os do carnívoro.
b) Nos mamíferos, a saliva contém ptialina (amilase salivar), enzima que atua na digestão de polissacarídeos. A partir dessa informação, é correto afirmar que, nos herbívoros, a digestão química começa na boca e, nos carnívoros, começa apenas no estômago? Justifique sua resposta.
a) A dieta de mamíferos herbívoros é composta principalmente de fibras de celulose, e o processo de digestão desses animais apresenta uma série de modificações que permitem a utilização de celulose como fonte de energia. Uma vez que a catálise da quebra das ligações que mantém unidas as moléculas de glicose na celulose não é efetuada por enzimas produzidas por mamíferos, os herbívoros mantém, ao longo do seu intestino, grandes quantidades de bactérias e protozoários anaeróbicos que promovem a quebra da celulose. Dessa forma, o comprimento do intestino desses animais é significativamente maior, o que permite o abrigo desse imenso contingente de microorganismos. Além disso, nota-se, em herbívoros, a presença de grandes divertículos intestinais (chamados também de cecos) em cujo interior também se nota a presença de microorganismos fermentadores.
b) Sim, é correto. Em herbívoros, nos quais a dieta é composta exclusivamente de vegetais, a digestão química do amido tem início na boca. Nesses animais, há grandes molares que proporcionam a maceração da matéria vegetal, aumentando o tempo de mastigação e possibilitando, assim, a ação efetiva da amilase salivar sobre o substrato.
No que se refere aos carnívoros, não há consenso na literatura sobre a presença de amilase na saliva. De qualquer modo, a observação da dentição de um carnívoro típico revela a progressiva modificação do conjunto de dentes molares (maceradores) em um sistema de corte (dentes carniceiros – figura abaixo).
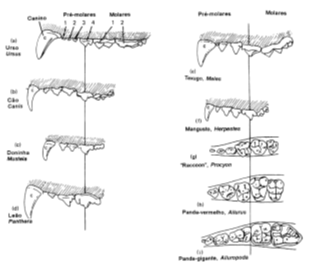
etirado de Harvey, P. F, J. B. Heiser & W. N. McFarland. A Vida dos Vertebrados. 1993. Ed. Atheneu.
Portanto, a mastigação, num carnívoro típico, pode ser considerada desprezível. Dessa forma, mesmo se considerarmos a existência de amilase na saliva de um carnívoro (aceitando, assim, a informação do enunciado), a ação dessa enzima sobre eventuais carboidratos será desprezível.
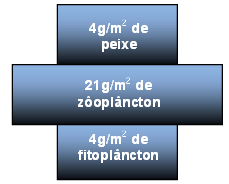
As pirâmides ecológicas são utilizadas para representar os diferentes níveis tróficos de um ecossistema e podem ser de três tipos: número de indivíduos, biomassa ou energia. Elas são lidas de baixo para cima e o tamanho dos retângulos é proporcional à quantidade que expressam.
Considere uma pirâmide com a seguinte estrutura:
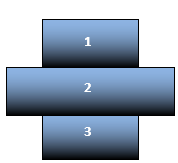
a) Que tipo de pirâmide, entre os três tipos citados no texto, não poderia ser representada por essa estrutura? Por quê?
b) Dê um exemplo de uma pirâmide que pode ser representada pela estrutura indicada. Substitua 1, 2 e 3 por dados quantitativos e qualitativos que justifiquem essa estrutura de pirâmide.
a) Dentre os tipos de pirâmides citados no texto, o único que não pode ser representado pela figura é a pirâmide de energia. Esse tipo de pirâmide representa o fluxo de energia através dos níveis tróficos de uma cadeia alimentar. A energia que sustenta toda a cadeia é proveniente da conversão de energia luminosa em química, promovida pela fotossíntese, efetuada pelos produtores. Neste primeiro nível trófico, além da assimilação de energia, há a utilização de parte da energia para a manutenção da vida da própria população vegetal, além da perda de energia que ocorre durante os processos metabólicos. Com isso, a quantidade de energia efetivamente disponível para o segundo nível trófico, composto pelos consumidores primários, é necessariamente menor que aquela assimilada pelos produtores. Da mesma forma, os consumidores primários vão armazenar apenas parte da energia que conseguem a partir do primeiro nível trófico. Outra fração será utilizada para a sustentação de sua vida ou será perdida. Com isso, a energia disponível para o próximo nível trófico (composto pelos consumidores secundários – carnívoros) será ainda menor. A representação gráfica da quantidade de energia em cada nível trófico corresponderá a uma pirâmide na qual cada nível corresponde a uma barra que é menor – denotando menos energia disponível – que a barra relacionada ao nível imediatamente inferior.
b) O candidato poderia utilizar, como exemplo, uma pirâmide de números. Nela, cada nível da pirâmide representa o número de indivíduos nas populações de cada nível trófico componente de uma cadeia alimentar. Considerando uma cadeia alimentar como planta → pulgões → pássaro, teríamos:
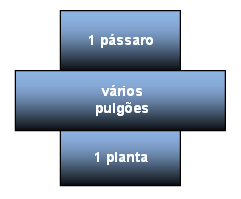
O candidato poderia, alternativamente, utilizar-se de um exemplo envolvendo uma pirâmide de biomassa para comunidades aquáticas. Nelas pode-se ter, devido à variações na taxa de reprodução do fitoplâncton, situações em que a biomassa total do fitoplâncton é menor que aquela do zooplâncton, componente do nível trófico imediatamente superior. Com isso teríamos:
 .
.
Lâmpadas incandescentes, como as de 60 W, têm uma data-limite no Brasil para fabricação e importação. Para sua substituição são recomendadas as lâmpadas fluorescentes, mais econômicas, embora as incandescentes reproduzam mais fielmente a luz natural, produzida no Sol e filtrada pela atmosfera terrestre.
A lâmpada incandescente tem em seu interior um filamento de tungstênio (W). A lâmpada fluorescente mais comum contém mercúrio (Hg), de massa molar 200 g/mol, que é uma substância tóxica, cujo limite máximo de seu vapor, estabelecido pela Organização Mundial da Saúde (OMS), é 0,04 mg por m3 de ar no ambiente de trabalho.
(www.brasil.gov.br. Adaptado.)
a) Com base nas posições dos metais W e Hg na Classificação Periódica dos Elementos Químicos, qual deles apresenta maior ponto de fusão e maior massa específica (densidade absoluta)? Justifique sua resposta.
b) Em um galpão isolado e totalmente vazio, foi quebrada uma lâmpada fluorescente contendo 1,0 × 10−4 mol de Hg. Sabendo-se que todo o Hg vaporizou-se, distribuindo-se uniformemente pelo ar ambiente e atingindo o limite máximo estabelecido pela OMS, calcule o volume ocupado pelo ar no interior do galpão.
a) Considerando que o ponto de fusão é uma propriedade periódica que apresenta a seguinte variação, em função do número atômico:
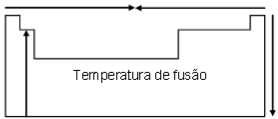
O elemento W apresenta o maior ponto de fusão, por estar mais abaixo e ao centro da tabela periódica.
Com relação a massa específica, que também é uma propriedade periódica, o W apresenta o maior valor pois está localizado mais abaixo e ao centro da tabela periódica, conforme figura abaixo:
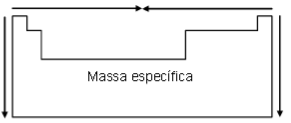
b) A massa m de de Hg é dada por:
| 1 mol Hg |  |
200 g |
| Hg |  |
m |
Sendo o limite máximo do vapor de Hg igual a 0,04 mg/m3, temos que o volume V do galpão pode ser calculado por:
| 0,04 mg |  |
1 m3 |
| 20 mg |  |
V |
O bicarbonato de sódio em solução injetável, indicado para tratamento de acidose metabólica ou de cetoacidose diabética, é comercializado em ampolas de 10 mL, cuja formulação indica que cada 100 mL de solução aquosa contém 8,4 g de NaHCO3.
Uma análise mostrou que o conteúdo das ampolas era apenas água e bicarbonato de sódio; quando o conteúdo de uma ampola desse medicamento reagiu com excesso de HCl, verificou-se que foi produzido 8,0 × 10–3 mol de gás carbônico, uma quantidade menor do que a esperada.
a) Utilizando R = 0,08 atm L K–1 mol–1, calcule a pressão exercida pelo gás liberado na análise do medicamento, quando confinado em um recipiente de 96 mL a 300 K.
b) Considerando a equação para reação entre o bicarbonato de sódio e o ácido clorídrico,
NaHCO3 (aq) + HCl (aq) → NaCl (aq) + CO2 (g) + H2O (l) determine a porcentagem em massa de bicarbonato de sódio presente na ampola analisada, em relação ao teor indicado em sua formulação. Apresente os cálculos efetuados.
a) Utilizando os dados fornecidos e a equação dos gases ideais , temos:
b) Pelas proporções estequiométricas da reação, para cada mol de CO2 formado, um mol de NaHCO3 é consumido. Por isso, foram consumidos de NaHCO3. Sabendo a massa molar do NaHCO3, podemos então encontrar a massa de bicarbonato consumida.
Observe que o teor de bicarbonato indicado é de , enquanto que o teor encontrado é de . Finalmente, o teor relativo pedido é:
Sob a forma gasosa, o formol (CH2O) tem excelente propriedade bactericida e germicida. O gráfico representa a variação de entalpia na queima de 1 mol de moléculas de formol durante a reação química.
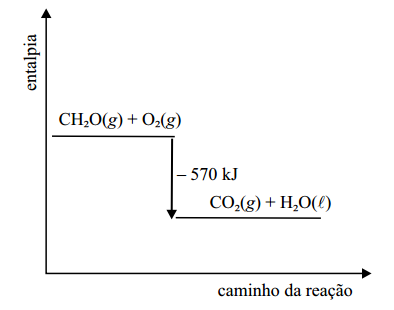
a) Escreva a fórmula estrutural do formol e o nome da função orgânica presente nas moléculas desse composto.
b) Dadas as entalpias-padrão de formação do e do , calcule a entalpia-padrão de formação do formol.
a) A fórmula estrutural do formol é:
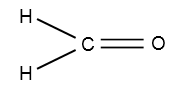
A função orgânica do formol é o aldeído, já que há um grupo C=O ligado a uma cadeia alifática.
b) Através do enunciado, temos conhecimento das variações de entalpia das seguintes reações:
Perceba que invertendo a última reação e somando-a às duas primeiras, teremos:
A reação acima é justamente a reação padrão de formação do formol, e sua variação de entalpia é:
A figura representa uma pilha formada com os metais Cd e Ag, mergulhados nas soluções de Cd(NO3)2(aq) e AgNO3(aq), respectivamente. A ponte salina contém solução de KNO3(aq).
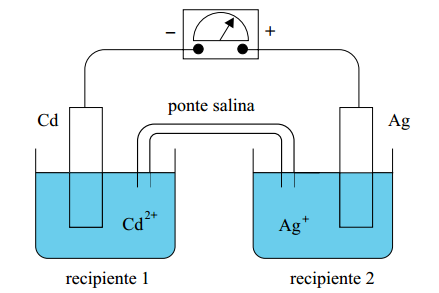
a) Sabendo que a diferença de potencial da pilha, nas condições padrão, é igual a +1,20 V e que o potencial padrão de redução do cádmio é igual a –0,40 V, calcule o potencial padrão de redução da prata. Apresente seus cálculos.
b) Para qual recipiente ocorre migração dos íons K+ e NO3- da ponte salina? Justifique sua resposta.
a) A partir da figura, conclui-se que o cátodo (eletrodo positivo e onde ocorre a redução) é representado pela Ag e consequentemente o ânodo (eletrodo negativo e onde ocorre a oxidação) é representado pelo Cd. Temos que o eletrodo de prata apresenta o maior potencial padrão de redução (), sendo assim:
b) Sabe-se que a função da ponte salina é manter o equilíbrio iônico da pilha. Portanto, a ponte salina é responsável pelo transporte de íons. Durante o funcionamento da pilha ocorre um desbalanceamento de cargas nas semi-celas de oxidação e de redução. Assim, na semi-cela de oxidação (ânodo) ocorre a seguinte reação
o que promove um aumento na concentração de íons no meio. Na semi-cela de redução (cátodo) temos a reação e verifica-se uma diminuição na concentração de íons .
Finalmente, os íons da ponte salina migram para promover o equilíbrio iônico na pilha: os íons K+ migram para o cátodo, para compensar a diminuição de íons positivos, pois a concentração de Ag+ diminui enquanto que a concentração do ânion presente na solução do cátodo permanece a mesma. Isso faz com que a solução tenda a apresentar carga negativa e atraia o cátion da ponte salina; os íons nitrato migram para o ânodo, pois a concentração de aumenta, fazendo com que a solução tenda a apresentar carga positiva, o que atrai os ânions.
Os compostos 1 e 2, representados nas figuras, são compostos orgânicos utilizados como solventes na indústria química e farmacêutica.
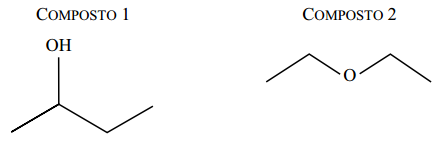
Na tabela, cada letra (x, y, z, w) pode representar somente o composto 1 ou o composto 2.
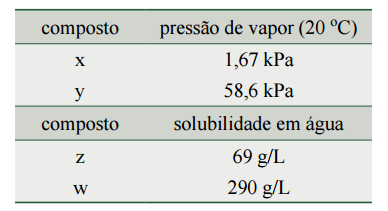
a) Identifique os compostos x, y, z e w.
b) Que tipo de isomeria ocorre entre os compostos 1 e 2? Escreva o nome oficial do composto que apresenta atividade ótica.
a) A pressão de vapor é definida como a pressão exercida pelos vapores de um líquido sobre as paredes do recipiente e sobre sua superfície.
Sendo assim, a maior pressão de vapor será verificada para a substância mais volátil, que no caso é o composto 2, pois é polar e apresenta interações intermoleculares do tipo dipolo permanente. O composto 1 também é polar, mas realiza interações intermoleculares mais intensas, do tipo ligação de hidrogênio.
Assim:
x = 1 e y = 2.
Com relação à solubilidade, deve-se levar em consideração, também, a questão das interações intermoleculares realizadas pelos compostos. O composto 1, como explicado anteriormente, realiza interações mais intensas e, portanto é o que apresenta a maior solubilidade de em água.
Assim:
z = 2 e w = 1.
b) A isomeria é caracterizada por compostos distintos apresentarem a mesma fórmula molecular.
Neste caso, possuem a fórmula molecular C4H10O e a isomeria que ocorre é a isomeria plana de função, tendo em vista que o primeiro composto é um álcool e o segundo um éter.
O composto que apresenta atividade ótica deve possuir carbono assimétrico (4 ligantes diferentes – C*). Neste caso, o composto 1 apresenta carbono assimétrico, como mostra a figura abaixo:
O nome do composto é butan-2-ol. Uma possibilidade que o candidato poderia apresentar como nomenclatura é 2-butanol, embora esta nomenclatura não seja utilizada atualmente pela IUPAC.