
Questão 3 Fuvest 2026 - 2ª fase - dia 2
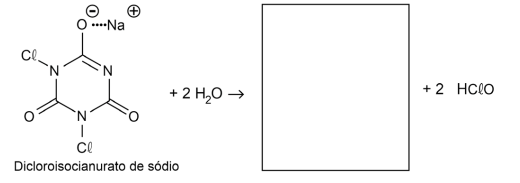
Produtos que contêm íons hipoclorito () e ácido hipocloroso () podem ser utilizados para desinfetar ambientes. Para o tratamento de piscinas também pode ser utilizado o dicloroisocianurato de sódio (estrutura representada na folha de respostas), um sal que, ao ser solubilizado em água, produz ácido hipocloroso e um outro produto.
a) Escreva a estrutura do outro produto formado nessa reação no quadro da folha de respostas.
Folha de resposta
Água sanitária é uma solução diluída de íons hipoclorito, gerada a partir da reação de gás cloro com íons hidróxido, formando também íons cloreto e água. Apesar de o gás cloro ser tóxico, usar a água sanitária para limpeza é seguro, porém deve-se tomar cuidado para não a misturar com outros agentes de limpeza, como desinfetantes a base de amoníaco ou vinagre. A mistura com desinfetantes a base de amônia pode gerar cloroaminas tóxicas solúveis em água, como
b) Escreva o equilíbrio de formação do íon hipoclorito a partir do gás cloro em meio básico e explique, a partir desse equilíbrio, por que a adição de vinagre à água sanitária pode ser nociva à saúde.
c) Desenhe a estrutura de Lewis da molécula de e justifique sua solubilidade em água com base na sua geometria.
Note e adote:
Distribuição eletrônica para
N:
Cℓ:
a) O dicloroisocianurato de sódio é um sal que ao se solubilizar em água, ocorre a hidrólise, formando como um dos produtoso :
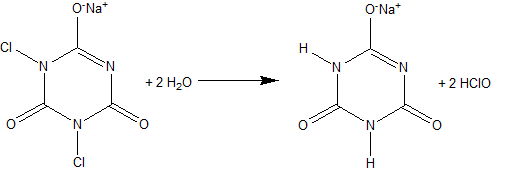
Ocorre substituição dos átomos de cloro por hidrogênio na molécula orgânica.
b) O equilíbrio de formação do íon hipoclorito () a partir do gás cloro () em meio básico () pode ser equacionado como:
O vinagre é uma solução aquosa de ácido acético (), que é um ácido fraco. A adição de vinagre à água sanitária (que é básica devido à presença de e tem íons hipoclorito ) resulta na reação de H+ do ácido com OH- do equilíbrio. Assim, a concentração de diminui e o equilíbrio de formação do íon hipoclorito () é deslocado para a esquerda (sentido dos reagentes) pela diminuição da concentração de (Princípio de Le Chatelier), formando gás cloro () que é tóxico.
Portanto, a adição de vinagre (ácido) à água sanitária libera gás cloro (), um gás tóxico.
c) A estrutura de Lewis da molécula de é:
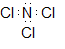
O N central faz 3 ligações com os 3 Cℓ e há um par de elétrons livres, sendo a geometria da molecula piramidal. Devido a essa geometria, os vetores de dipolo das ligações polares N-Cℓ não se anulam, portanto, a molécula é polar.
A água () é uma molécula também polar (devido à diferença de eletronegatividade entre O e H e sua geometria angular). Como o é uma molécula polar, ela interage com as moléculas polares de água, o que justifica a solubilidade em água.