
Questão 16 Unesp 2026 - 2ª fase
A bauxita é o principal minério de alumínio. A partir desse minério, obtêm-se diversos compostos de alumínio, dentre eles o hidróxido de alumínio, , a partir do qual se obtém o sulfato de alumínio, . O principal uso desse sulfato ocorre nas estações de tratamento de água (ETA). Outro composto obtido a partir do é a alumina, , a partir da qual é obtido o alumínio metálico, , por eletrólise ígnea. O esquema resume essas informações.
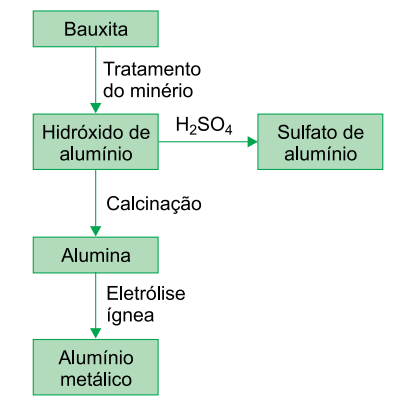
a) Escreva a equação balanceada da reação química que ocorre entre hidróxido de alumínio e ácido sulfúrico produzindo sulfato de alumínio e água. Qual é a função desse sal nas estações de tratamento de água?
b) Represente a distribuição eletrônica em camadas do íon . Considerando a constante de Faraday igual a , calcule a quantidade de carga elétrica, expressa em Coulombs, necessária para produzir 54 kg de alumínio metálico pela eletrólise ígnea da alumina.
a) A reação entre hidróxido de alumínio, , e ácido sulfúrico, , é uma reação de neutralização que forma o sal de sulfato de alumínio e água conforme a reação:
O sulfato de alumínio é um sal que atua como coagulante ou floculante no tratamento de água. Ele reage com a água ou do meio para formar um hidróxido de alumínio () que atrai e aglutina as partículas suspensas (impurezas, argila, matéria orgânica) presentes na água bruta, formando flocos maiores que podem ser facilmente removidos por decantação e filtração
b) O elemento alumínio possui 13 prótons (número atômico, Z), portanto, no estado neutro (carga nula) também possui 13 elétrons. Através do diagrama de distribuição eletrônica ("diagrama de Pauling"), temos:
Para formar o cátion trivalente (carga +3), o átomo de alumínio perde os três elétrons menos atraídos pelo núcleo, isto é, os três elétrons da camada de valência (nível 3):
Com base na distribuição eletrônica por subníveis apresentada acima, podemos expressar a distribuição eletrônica por camadas agrupando o total de elétrons em cada nível:
Desse modo, a distribuição eletrônica por camadas será:
Na eletrólise ígnea da alumina, , o cátion alumínio sofre redução conforme a reação a seguir:
Pela estequiometria da reação, cada 3 mols de elétrons que atravessa o sistema é capaz de formar 1 mol de alumínio metálico. Sendo a constante de Faraday (9,65·104 C/mol) equivalente à carga de 1 mol de elétrons e a massa molar do alumínio de 27 g/mol, para formar 54 kg (54.103 g) de alumínio temos:
Portanto, a quantidade de carga elétrica necessária para produzir 54 kg de alumínio metálico pela eletrólise ígnea da alumina é de 5,79×108 C.